中国瓣膜出海新突破,VenusP-Valve PROTEUS研究获美国医保覆盖
近日, 启明医疗国际化拳头产品VenusP-Valve经导管人工肺动脉瓣膜置换系统(TPVR)PROTEUS临床研究,获美国联邦医疗保险和联邦医疗补助服务中心(Centers for Medicare & Medicaid Services ,CMS)批准纳入医保。
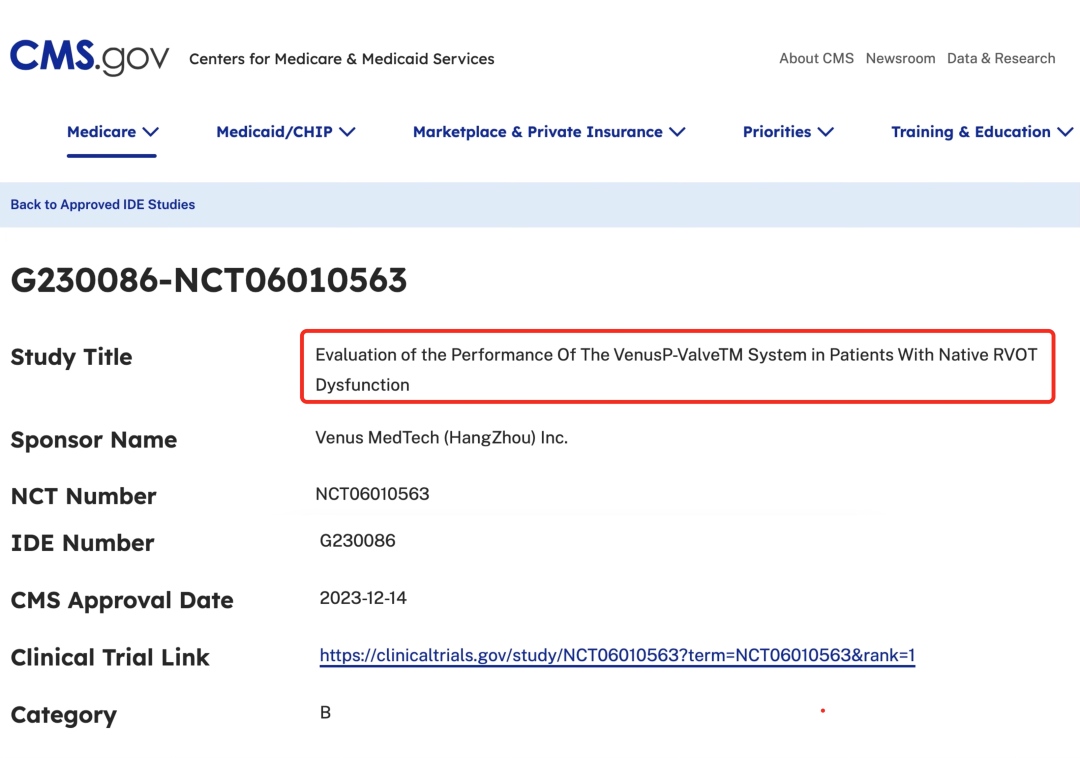
此次获批准意味着,所有符合CMS相关医疗保险计划的受益者,在参加VenusP-Valve PROTEUS研究时均可以享受到接受VenusP-Valve治疗所对应的报销。这是今年继获法、德两大核心欧洲市场医保准入后,VenusP-Valve在全球最大医疗市场美国获得的又一大突破。
*美国联邦医疗保险和联邦医疗补助服务中心(CMS)隶属于美国卫生及公共服务部(Department of Health and Human Services, HHS),负责管理医疗保险计划,并与州政府合作管理医疗补助计划、国家儿童健康保险计划以及健康保险标准等。作为一个公共医疗保险服务平台,CMS为全美超1.6亿人群提供医疗保险与医疗补助服务。
此前,VenusP-Valve已获美国食品药品监督管理局(FDA)批准其研究性器械豁免(IDE)申请,成为首个获得FDA批准进行临床研究的中国产人工心脏瓣膜。今年11月,VenusP-Valve又获美国首家中心加州大学洛杉矶分校成人先天性心脏病中心(Ahmanson/UCLA Adult Congenital Heart Disease Center)伦理批件,美国关键性临床试验入组启动在即。
作为中国及欧洲首个获批上市的自膨胀式TPVR产品,VenusP-Valve已于2022年4月8日获得欧盟CE MDR认证,是首个在新法规下获批的III类心血管植入类医疗器械。截至目前,VenusP-Valve已覆盖中国、英国、意大利、西班牙、丹麦、希腊、法国、德国、波兰、瑞士等全球五十余个主流国家,并持续在新覆盖的医疗机构实现手术植入。
今年以来,VenusP-Valve连获沙特、土耳其、泰国、摩洛哥、约旦、卡塔尔、乌拉圭、埃及、巴基斯坦、哥伦比亚等多国上市许可,在国际市场进展连连,助力公司全面深化国际化进程。
VenusP-Valve
VenusP-Valve具备显著的临床价值。其独特的双喇叭口设计,流出端的裸支架设计保障分支血流,稳定的多部位锚定特点,释放简便,植入前无需预先放置固定支架。瓣膜尺寸规格多,适用范围广,在临床上可以满足超过85%大尺寸肺动脉瓣膜患者的需求。
相关临床数据证明了该产品的长期安全性和有效性,并得到了国内外专家的高度认可。VenusP-Valve欧洲三年期随访数据显示,64名接受TPVR手术的患者(尚有部分患者由于新冠疫情未能计入)手术成功率为100%,全因死亡率及手术再干预率均为0,所有患者均未出现中度或重度肺动脉瓣反流;96.87%受试者的瓣周漏及三尖瓣反流在轻度以内。
声明
*本文披露内容仅作信息交流、学术讨论之目的,在任何情况下均不得被视为医疗建议或超出前述目的之用途。我司对文中信息的完整性、准确性或及时性不做任何陈述或保证。
*本文提及的任何医疗器械,我司不对其在诊疗行为中的性能、临床表现等做任何承诺及保证。
*中文启明医疗,VENUSMEDTECH,设计过的图形启,VenusP-Valve等是杭州启明医疗器械股份有限公司名下商标。
Copyright 2023杭州启明医疗器械股份有限公司版权所有。